L'ApoB est la principale protéine présente sur chaque particule de lipoprotéine athérogène (LDL, VLDL, IDL, Lp(a)) — une particule, une molécule d'ApoB. Il s'agit donc d'un comptage direct des particules, ce qui, d'un point de vue mécanistique, est plus révélateur que la seule concentration en cholestérol LDL.
The 2024 National Lipid Association Expert Consensus proposed stratified ApoB targets: <90 mg/dL for intermediate-risk, <70 mg/dL for high-risk, and <60 mg/dL for very high-risk patients — thresholds consistent with epidemiological data and treatment effects observed in lipid-lowering trials. In a 2024 analysis of over 500,000 UK Biobank participants, when LDL-C and ApoB were discordant, cardiovascular risk followed ApoB — not LDL-C. Elevated ApoB was also independently associated with increased Alzheimer's disease risk.
Références :
Handelsman Y, et al. Déclaration de consensus de l'Association américaine d'endocrinologie clinique sur la prise en charge de la dyslipidémie. Endocr Pract. 2024.
Ibanez B, et al. Méta-analyse du cholestérol LDL et de l'athérosclérose chez les personnes présentant un risque optimal. J Am Coll Cardiol. 2021.

L'abandon des objectifs standard en matière de LDL-C dans le domaine de la longévité s'explique en partie par un changement dans la mesure effectuée — qui privilégie désormais le nombre de particules (ApoB) — et en partie par un abaissement du seuil absolu. Une méta-analyse majeure a démontré que, même chez les personnes dont tous les facteurs de risque cardiovasculaire se situaient dans la fourchette optimale, il existait une corrélation significative entre la concentration en LDL-C et la présence d'athérosclérose.
Ibanez et al. (2021) : Chez les personnes présentant des valeurs optimales pour tous les facteurs de risque cardiovasculaire, on a observé une corrélation significative entre la concentration en LDL-C et l'athérosclérose subclinique, ce qui suggère qu'il n'existe pas de taux de LDL-C véritablement sans risque du point de vue de la formation de plaques.
Références :
Ibanez B, et al. Athérosclérose subclinique et LDL-C chez les individus à risque optimal. J Am Coll Cardiol. 2021;77(24):3031–3041.
Ridker PM, et al. La rosuvastatine dans la prévention des événements vasculaires chez les hommes et les femmes présentant un taux élevé de protéine C-réactive (étude JUPITER). N Engl J Med. 2008 ; 359(21) : 2195-207.

Contrairement à tous les autres biomarqueurs mentionnés dans cet article, le taux de Lp(a) ne peut pas être modifié par le mode de vie. Les taux de Lp(a) sont déterminés à environ 70 à 90 % par la génétique et restent stables tout au long de la vie, ce qui fait d’un taux élevé de Lp(a) un facteur de risque cardiovasculaire permanent. Dans le domaine de la longévité, on le considère comme un test fondamental à réaliser une seule fois, qui permet de réévaluer lifetime et justifie une prise en charge plus rigoureuse de tous les autres facteurs modifiables.
Étude de population générale de Copenhague (randomisation mendélienne, n = 40 486) : un taux élevé de Lp(a) d'origine génétique était associé à une augmentation de 22 % du risque d'infarctus du myocarde pour chaque doublement des taux de Lp(a).
Méta-analyse au niveau des participants portant sur six essais cliniques sur les statines contrôlés par placebo : le Lp(a) et le LDL-C prédisent de manière indépendante et additive le risque d'ASCVD — ce qui signifie qu'un taux élevé de Lp(a) entraîne un risque résiduel significatif, même chez les patients dont le LDL-C est bien contrôlé.
The EAS 2022 consensus: the association between Lp(a) and ASCVD outcomes is continuous. The clinical cutoffs of <30 mg/dL and >50 mg/dL are pragmatic rather than biological. An Lp(a) of 100 mg/dL approximately doubles ASCVD risk, with the absolute increase substantially greater in higher-baseline-risk individuals.
Nouveau traitement : lors des essais de phase II, le pelacarsen (oligonucléotide antisens) a permis de réduire le taux de Lp(a) jusqu’à 80 % à la dose la plus élevée, 98 % des patients atteignant des taux inférieurs à 50 mg/dL. L’essai de phase III Lp(a)HORIZON, portant sur les résultats cardiovasculaires, est en cours.
La mise à jour ciblée de la NLA de 2024 recommande de mesurer le taux de Lp(a) au moins une fois chez chaque adulte — une position désormais partagée par l'EAS, l'ACC/AHA et l'ESC.
Références :
Nordestgaard BG, et al. La lipoprotéine (a) en tant que facteur de risque cardiovasculaire : état des lieux. Eur Heart J. 2010 ; 31(23) : 2844-53.
Tsimikas S, et al. Traitement antisens ciblant l'apolipoprotéine (a) : une étude de phase I randomisée, en double aveugle et contrôlée par placebo. Lancet. 2015 ; 386(10002) : 1472-83.
Ridker PM, et al. Lipoprotéine (a), LDL-C et hs-CRP : résultats cardiovasculaires sur 30 ans chez les femmes. N Engl J Med. 2024.
Handelsman Y, et al. Mise à jour ciblée 2024 de la NLA. J Clin Lipidol. 2024.

L'HbA1c reflète la glycémie moyenne des 2 à 3 derniers mois. Les études sur les centenaires montrent systématiquement que l'HbA1c est restée inférieure à 6 % tout au long de la vie, la mortalité toutes causes confondues la plus faible chez les populations non diabétiques étant observée dans la fourchette de 5,0 à 5,6 % (données NHANES III). L'objectif optimisé pour la longévité, compris entre 5,0 et 5,4 %, reflète ces données. Remarque : la limite inférieure de 5,0 % est importante — les données NHANES montrent une relation en forme de U chez les non-diabétiques, un taux d'HbA1c inférieur à 5,0 % étant associé à une mortalité accrue, ce qui reflète probablement une anémie, une maladie hépatique ou d'autres pathologies confondantes plutôt qu'un contrôle métabolique bénéfique.
Ensemble de données NHANES III : les participants ne souffrant pas de diabète et présentant un taux d'HbA1c compris entre 5,0 et 5,6 % constituaient la catégorie de référence présentant la mortalité toutes causes confondues la plus faible. Le diabète non diagnostiqué (HbA1c > 6,5 %) était associé à un risque de mortalité toutes causes confondues 1,3 fois plus élevé.
Cohorte de centenaires (Catalogne) : les biomarqueurs liés au métabolisme du glucose — notamment l'HbA1c et la glycémie à jeun — ont eu un impact négatif significatif sur la probabilité d'atteindre un âge très avancé lorsqu'ils se situaient dans les quintiles les plus élevés.
Nuance importante : l'essai clinique randomisé ACCORD a montré qu'une réduction pharmacologique intensive du taux d'HbA1c en dessous de 6,5 % chez les patients atteints d'un diabète de type 2 établi entraînait une augmentation de la mortalité — attribuée à l'hypoglycémie résultant d'un traitement médicamenteux agressif. L'objectif en matière de longévité est d'obtenir naturellement un faible taux d'HbA1c grâce à une bonne santé métabolique, et non par une suppression pharmacologique chez les patients fragiles ou diabétiques.
Références :
Selvin E, et al. Hémoglobine glyquée, diabète et risque cardiovasculaire chez les adultes non diabétiques. N Engl J Med. 2010 ; 362(9) : 800-11.
Groupe d'étude ACCORD. Effets d'un traitement hypoglycémiant intensif dans le diabète de type 2. N Engl J Med. 2008 ; 358(24) : 2545-59.
Ponjoan A, et al. Profil des biomarqueurs chez les centenaires dans une cohorte issue de la population générale. GeroScience. 2023.
Carson AP, Fox CS, McGuire DK, et al. Faible taux d'hémoglobine A1c et risque de mortalité toutes causes confondues chez les adultes américains non diabétiques. Circ Cardiovasc Qual Outcomes. 2010 ; 3(6) : 661-667

Les plages de référence standard en laboratoire pour l'insuline à jeun sont particulièrement larges. Les plages de référence actuelles ne considèrent pas qu'il y a hyperinsulinémie tant que le taux d'insuline à jeun ne dépasse pas 24,9 µIU/mL — soit un niveau trois à cinq fois supérieur à celui que les cliniciens spécialisés dans la longévité jugent optimal. Un taux élevé d'insuline à jeun constitue un signe précurseur de l'insulinorésistance avant même l'HbA1c, apparaissant souvent plusieurs années avant que le dérèglement glycémique ne devienne manifeste.
Méta-analyse prospective (Zhang et al., Bioscience Reports, 2017) : chaque augmentation d'une unité du taux d'insuline à jeun, dans les limites de la normale, était associée à une augmentation de 5 % du risque cardiovasculaire. Les personnes présentant un taux d'insuline à jeun inférieur à 5 µIU/mL affichaient une mortalité cardiovasculaire et une mortalité toutes causes confondues significativement plus faibles. Xun et al. ont montré que chaque augmentation de 50 pmol/L de l'insuline à jeun était associée à une augmentation de 25 % du risque d'hypertension et de 16 % du risque de maladie coronarienne.
Références :
Zhang X, et al. Insuline à jeun, résistance à l'insuline et risque d'hypertension dans la population générale. Bioscience Reports. 2017 ; 37(5) : BSR20160343.
Sung KCC, Seo MHH, Rhee EJJ, Wilson AM. Un taux élevé d'insuline à jeun permet de prédire l'incidence future du syndrome métabolique : une étude de suivi sur 5 ans. Cardiovasc Diabetol. 2011 ; 10(1) : 108. doi:10.1186/1475-2840-10-108
Xun P, Wu Y, He Q, He K. Concentrations d'insuline à jeun et incidence de l'hypertension, des accidents vasculaires cérébraux et des maladies coronariennes : une méta-analyse d'études de cohortes prospectives123. The American Journal of Clinical Nutrition. 2013 ; 98(6) : 1543-1554.

Si le seuil clinique du prédiabète commence à 100 mg/dL, les données issues d'études de cohorte prospectives montrent qu'une glycémie à jeun comprise entre 90 et 99 mg/dL est associée à une augmentation progressive du risque cardiovasculaire et métabolique par rapport à des taux inférieurs à 90 mg/dL. Dans le domaine de la longévité, cette fourchette est considérée comme un signal d'alerte précoce plutôt que comme un résultat normal rassurant.
Références :
Levitan EB, et al. L'hyperglycémie non diabétique est-elle un facteur de risque de maladie cardiovasculaire ? Arch Intern Med. 2004 ; 164(19) : 2147-55.
Rijkelijkhuizen JM, et al. Seuils optimaux pour la glycémie à jeun et le risque cardiovasculaire associé. Diabetes Care. 2007 ; 30(5) : 1167-72.
Bao C, Zhang D, Sun B, et al. Seuils optimaux de glycémie à jeun pour une stratégie en deux étapes visant à estimer la prévalence et à dépister le diabète et le prédiabète non diagnostiqués à Harbin, en Chine. PLOS ONE. 2015 ; 10(3) : e0119510.
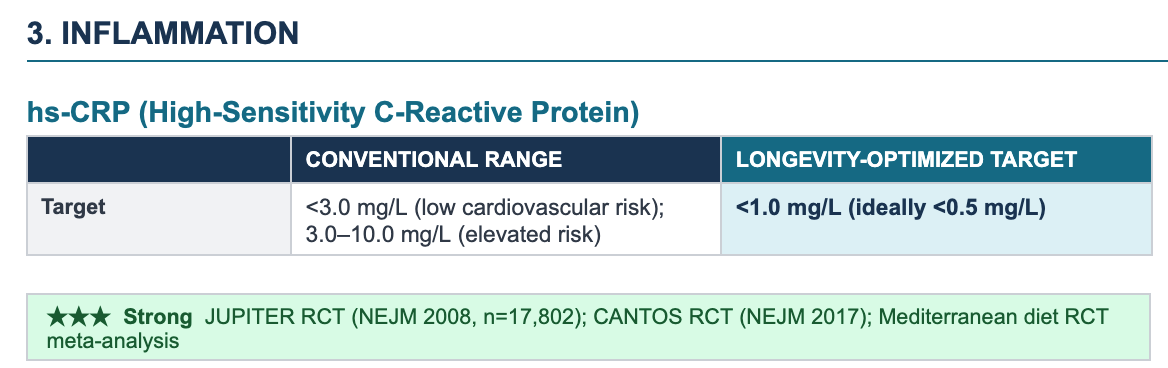
Les données issues d'essais cliniques randomisés (ECR) les plus déterminantes proviennent de l'étude phare JUPITER : une étude randomisée et contrôlée par placebo menée auprès de 17 802 hommes et femmes en bonne santé apparente, qui a établi que la hs-CRP constituait un marqueur de risque cardiovasculaire indépendant et exploitable, même chez les patients présentant un taux normal de cholestérol LDL.
JUPITER within-trial dose-response analysis: participants who achieved hs-CRP below 1 mg/L on rosuvastatin saw a 79% reduction in cardiovascular events — substantially more than those who achieved LDL-C reduction alone, firmly establishing <1 mg/L as the longevity-optimized target.
Méta-analyse des essais cliniques randomisés portant sur le régime méditerranéen : ce régime a réduit la CRP haute sensibilité (hs-CRP) de 0,98 mg/L en moyenne ; un régime riche en fibres a réduit la hs-CRP de 28 %, un effet comparable à celui d'un traitement par 20 mg de lovastatine par jour.
Données sur les centenaires (PMC 2025) : les populations de centenaires présentent des taux plasmatiques de CRP nettement plus faibles (0,9 ± 0,4 mg/L) que les personnes âgées d'âge moyen (2,8 ± 1,6 mg/L), ces différences persistant même après prise en compte des comorbidités.
Références :
Ridker PM, et al. La rosuvastatine dans la prévention des événements vasculaires chez les hommes et les femmes présentant un taux élevé de protéine C-réactive (étude JUPITER). N Engl J Med. 2008 ; 359(21) : 2195-207.
Ridker PM, Danielson E, Fonseca FA, et al. Baisse des taux de protéine C-réactive et de cholestérol LDL ainsi que des taux d'événements cardiovasculaires après l'instauration d'un traitement par rosuvastatine : une étude prospective issue de l'essai JUPITER. The Lancet. 2009 ; 373(9670) : 1175-1182. doi:10.1016/S0140-6736(09)60447-5
Ridker PM, et al. Traitement anti-inflammatoire par canakinumab dans les maladies athéroscléreuses (CANTOS). N Engl J Med. 2017;377(12):1119–31.
Ridker PM, et al. Taux de protéine C-réactive et résultats après un traitement aux statines. N Engl J Med. 2005 ; 352(1) : 20-8.
Keshani M, Rafiee S, Heidari H, Rouhani MH, Sharma M, Bagherniya M. Le régime méditerranéen réduit l'inflammation chez les adultes : revue systématique et méta-analyse d'essais contrôlés randomisés. Nutr Rev. Publié en ligne le 10 novembre 2025 : nuaf213. doi:10.1093/nutrit/nuaf213
Adibi S. Un cadre conceptuel de santé numérique pour l'optimisation de la longévité : une approche centrée sur l'inflammation intégrant les données sur le microbiome et le mode de vie — Une revue et une proposition de plateforme. Nutrients. 2026 ; 18(2) : 231.

Les données prospectives établissent systématiquement un lien entre un taux d'homocystéine supérieur à 9–10 µmol/L et la mortalité d'origine cardiovasculaire et neurodégénérative. Cependant, les données scientifiques concernant l'homocystéine sont plus complexes que celles relatives aux autres biomarqueurs présentés dans cet article.
Nygård et al. (NEJM, 1997) : chez les patients présentant une coronaropathie confirmée par angiographie, des taux d'homocystéine compris entre 9,0 et 14,9 µmol/L étaient déjà associés à un rapport de mortalité de 3,3 par rapport aux taux inférieurs à 9 µmol/L — ce rapport s'élevant à 9,9 pour les taux ≥ 20 µmol/L.
Méta-analyse PMC portant sur 12 études prospectives (n = 23 623) : en comparant les catégories présentant les taux d'homocystéine les plus élevés à celles présentant les taux les plus bas, la mortalité par maladie coronarienne a augmenté de 66 %, la mortalité cardiovasculaire de 68 %, et chaque augmentation de 5 µmol/L était associée à une hausse de 52 % de la mortalité par maladie coronarienne.
Mise en garde concernant les ECR : des essais phares — HOPE-2 (2006), NORVIT (2006) et VITATOPS (2010) — ont permis de réduire efficacement le taux d'homocystéine plasmatique grâce à une supplémentation en vitamines B, mais n'ont globalement pas réussi à diminuer les critères d'évaluation cardiovasculaires majeurs, notamment l'infarctus du myocarde, l'accident vasculaire cérébral ou la mortalité toutes causes confondues. Une méta-analyse ultérieure portant sur 19 ECR (n = 47 921) a montré que la supplémentation en vitamines B réduisait significativement le risque d'AVC, mais pas celui de MCV, d'IM, de MC ou de mortalité toutes causes confondues. Cela ne remet pas en cause la valeur de l'homocystéine en tant que biomarqueur de risque, mais incite à la prudence quant à l'hypothèse selon laquelle la normalisation pharmacologique seule améliorerait les résultats.
Références :
Nygård O, et al. Taux plasmatiques d'homocystéine et mortalité chez les patients atteints d'une maladie coronarienne. N Engl J Med. 1997 ; 337(4) : 230-6.
Lonn E, et al. Traitement visant à réduire le taux d'homocystéine et résultats chez les patients à haut risque (HOPE-2). N Engl J Med. 2006 ; 354(15) : 1567-77.
Clarke R, et al. Effets de la réduction des taux d'homocystéine à l'aide de vitamines B sur les maladies cardiovasculaires, le cancer et la mortalité par cause spécifique : méta-analyse de 8 essais randomisés. Arch Intern Med. 2010 ; 170(18) : 1622-31.
Collaboration sur les études relatives à l'homocystéine. Homocystéine et risque de cardiopathie ischémique et d'accident vasculaire cérébral : une méta-analyse. JAMA. 2002 ; 288(16) : 2015-2022. doi:10.1001/jama.288.16.2015
Peng H et al. Taux élevés d'homocystéine et risque de mortalité cardiovasculaire et toutes causes confondues : une méta-analyse d'études prospectives. J Zhejiang Univ Sci B. 2015 ; 16(1) : 78-86.

L'IL-6 est la cytokine pro-inflammatoire la plus étudiée dans le contexte du vieillissement biologique (« inflammaging »). Les plages de référence standard en laboratoire sont établies à partir de données démographiques et ne reflètent pas les taux associés à une longévité optimale.
Centenarian cohort data (PMC 2025): centenarians demonstrate significantly reduced plasma IL-6 (1.4 ± 0.6 pg/mL) compared to average-aging elderly individuals (3.2 ± 1.8 pg/mL, p<0.001). These differences persist after controlling for comorbidities, suggesting low inflammatory status is a characteristic feature of exceptional longevity.
Tylutka et al., Frontiers in Immunology (2024, PRISMA meta-analysis): the overall IL-6 concentration was significantly higher in patients with age-related diseases compared to controls (SMD 0.16, p<0.001). IL-6 demonstrated diagnostic utility as an independent predictor of age-related morbidity and mortality in elderly adults.
Randomisation mendélienne (npj Genomic Medicine, 2019) : la voie de signalisation de l'IL-6 a révélé des associations causales inverses avec la fibrillation auriculaire, les accidents vasculaires cérébraux, les maladies coronariennes et les anévrismes de l'aorte abdominale — et s'est avérée positivement associée à l'âge des parents au moment de leur décès (indicateur de longévité).
Références :
Tylutka A, et al. Taux d'IL-6, de TNF et d'IL-1β et maladies liées à l'âge : revue systématique et méta-analyse. Front Immunol. 2024 ; 15 : 1330386.
Collaboration (données sur les centenaires). Un cadre conceptuel de santé numérique pour l'optimisation de la longévité. PMC 2025.
Georgakis MK, et al. La signalisation de l'IL-6 dans les maladies cardiovasculaires, les troubles immunitaires et la longévité. npj Genomic Medicine. 2019.
Adibi S. Un cadre conceptuel de santé numérique pour l'optimisation de la longévité : une approche centrée sur l'inflammation intégrant les données sur le microbiome et le mode de vie — Une revue et une proposition de plateforme. Nutrients. 2026 ; 18(2) : 231.

L'IGF-1 présente des nuances que la plupart des biomarqueurs n'ont pas : un taux élevé n'est en aucun cas synonyme de meilleure santé. La relation avec la longévité suit une courbe en U : tant les taux très bas que les taux très élevés sont associés à un risque accru, tandis que les taux intermédiaires sont associés au taux de mortalité le plus faible.
Longo et al., Aging Cell (2022) — méta-analyse de 19 études de cohorte prospectives (n = 30 876) : l'analyse dose-réponse a révélé une relation en U entre l'IGF-1 et le rapport de risque (HR) de mortalité toutes causes confondues. La fourchette de 120 à 160 ng/mL était associée à la mortalité la plus faible. La comparaison entre un taux d'IGF-1 faible et un taux moyen a montré une augmentation significative de la mortalité toutes causes confondues (HR = 1,33, IC à 95 % : 1,14–1,57) ; la comparaison entre un taux élevé et un taux moyen a également montré une mortalité accrue (HR = 1,23, IC à 95 % : 1,06–1,44).
EPIC-Heidelberg (Mukama et al., J Clin Endocrinol Metab, 2023, étude prospective basée sur la population) : des taux élevés d'IGF-1 ont montré une association directe avec le risque de cancer du sein (HR 1,25) et de cancer de la prostate (HR 1,31). Les taux d'IGF-1 les plus bas comme les plus élevés étaient associés à un risque accru de décès par cancer, par maladie cardiovasculaire et toutes causes confondues — confirmant ainsi la relation en U au sein d'une vaste population européenne.
En résumé : visez un taux d'IGF-1 se situant dans la fourchette physiologique moyenne — ce qui s'obtient généralement grâce à un apport protéique suffisant mais modéré, à une activité physique régulière et à un sommeil de qualité — plutôt qu'une optimisation pharmacologique de l'axe GH/IGF-1.
Références :
Rahmani J, et al. Association entre les intervalles de concentration d'IGF-1 et la mortalité toutes causes confondues : une méta-analyse. Aging Cell. 2022 ; 21(2) : e13540.
Mukama T, et al. IGF-1 et risque de morbidité et de mortalité liées au cancer, aux maladies cardiovasculaires et à toutes causes confondues dans l'étude EPIC-Heidelberg. J Clin Endocrinol Metab. 2023 ; 108(10) : e1092–e1105.

Les données les plus solides proviennent d'une méta-analyse des données individuelles (IPD) publiée en 2023 dans *The Lancet Diabetes & Endocrinology* — l'une des plus vastes études jamais menées sur la fonction thyroïdienne — qui visait explicitement à définir les plages optimales de TSH et de FT4 en se basant sur les résultats cliniques plutôt que sur les percentiles statistiques de la population.
Xu et al., Lancet Diabetes & Endocrinology (2023), n = 134 346, suivi moyen de 11,5 ans : des associations non linéaires ont été identifiées pour la TSH, les 60e et 80e percentiles (médiane de 1,90 à 2,90 mIU/L) étant associés au risque le plus faible de MCV et de mortalité. La FT4 a montré une association en forme de J, les 20e–40e percentiles (médiane 13,5–14,8 pmol/L) présentant le risque le plus faible. La FT4 dans les 80e–100e percentiles était associée à une augmentation de 1,34 fois de la mortalité toutes causes confondues et à une augmentation de 1,57 fois de la mortalité par MCV par rapport à la fourchette optimale.
Interprétation : Le taux de TSH optimal pour la longévité ne se situe ni dans la partie basse de la fourchette (associée à une hyperthyroïdie subclinique et à un risque accru de maladies cardiovasculaires et de mortalité), ni à la limite supérieure conventionnelle de 4,0 mIU/L. C'est dans la fourchette de 1,9 à 2,9 mIU/L — que la plupart des cliniciens considèrent actuellement comme tout à fait normale — que le risque de mortalité est le plus faible. Chez les personnes âgées en particulier, une TSH dans la partie supérieure de la fourchette normale peut être adaptative plutôt que pathologique.
Références :
Xu Y, et al. Les plages optimales de fonctionnement thyroïdien définies en fonction du risque de maladies cardiovasculaires et de mortalité : revue systématique et méta-analyse des données individuelles des participants. Lancet Diabetes Endocrinol. 2023 ; 11(10) : 743-754. PMID : 37696273.
Razvi S, et al. Effet bénéfique de la L-thyroxine sur les facteurs de risque cardiovasculaire, la fonction endothéliale et la qualité de vie dans l'hypothyroïdie subclinique. J Clin Endocrinol Metab. 2007 ; 92(5) : 1715-23.

Les laboratoires standard ne signalent un « faible » taux de testostérone qu'à partir du seuil minimal de la population — un seuil statistique, et non un seuil optimisé pour la santé. La médecine de la longévité s'intéresse moins à éviter les « faibles » taux qu'à maintenir des niveaux associés à la santé métabolique, à la préservation de la masse musculaire, à la sensibilité à l'insuline et à la protection cognitive — ce qui correspond généralement à la partie supérieure de la fourchette moyenne pour l'âge concerné.
The Testosterone Trials (TTrials, NEJM 2016): in men 65+ with low testosterone (<275 ng/dL), testosterone treatment improved sexual function, physical function, and quality of life, with additional signals for bone density and anemia. Metabolic benefits were observed at levels in the mid-normal range.
Références :
Snyder PJ, et al. Effets d'un traitement à la testostérone chez les hommes âgés (TTrials). N Engl J Med. 2016 ; 374(7) : 611-624.
Araujo AB, Dixon JM, Suarez EA, Murad MH, Guey LT, Wittert GA. Revue clinique : Testostérone endogène et mortalité chez l'homme : revue systématique et méta-analyse. J Clin Endocrinol Metab. 2011 ; 96(10) : 3007-3019. doi:10.1210/jc.2011-1137

La médecine conventionnelle n'intervient que lorsque le DFG est inférieur à 60 ml/min/1,73 m². Le domaine de la longévité reconnaît que même un déclin subclinique dans la fourchette de 60 à 89 augmente considérablement le risque de mortalité cardiovasculaire et toutes causes confondues, ce qui fait d'un DFG supérieur à 90 un objectif à atteindre plutôt qu'une simple référence sans importance.
Consortium sur le pronostic de l'IRC (Lancet, 2010, n ≥ 1,1 million) : une association continue, indépendante et progressive a été observée entre une diminution du DFG estimé et une augmentation de l'albuminurie, d'une part, et la mortalité toutes causes confondues, la mortalité cardiovasculaire et l'insuffisance rénale, d'autre part — avec un surrisque significatif apparaissant dès un DFG estimé inférieur à 75 ml/min/1,73 m², et pas seulement au seuil de l'IRC fixé à 60.
Références :
Matsushita K, et al. Association entre le débit de filtration glomérulaire estimé et l'albuminurie, d'une part, et la mortalité toutes causes confondues et la mortalité cardiovasculaire, d'autre part, dans des cohortes issues de la population générale : une méta-analyse collaborative. Lancet. 2010 ; 375(9731) : 2073-81.

Les résultats des essais cliniques sur la vitamine D ont toujours été mitigés, mais les données étayant l'objectif de 40 à 60 ng/mL se sont considérablement renforcées grâce à des essais contrôlés randomisés récents.
Essai contrôlé randomisé TARGET-D (2024) : chez les patients à haut risque, une supplémentation en vitamine D ajustée pour atteindre des taux supérieurs à 40 ng/mL a réduit de manière significative le risque de récidive d'infarctus du myocarde — il s'agit de l'un des premiers essais contrôlés randomisés à démontrer un bénéfice cardiovasculaire spécifiquement lié à l'atteinte d'un taux cible supérieur à 40 ng/mL.
Essai clinique VITAL (NEJM, 2019, n = 25 871) : bien que les critères d'évaluation principaux n'aient pas montré de réduction significative, des analyses prédéfinies ont révélé une baisse significative de la mortalité par cancer chez les participants présentant un faible IMC — les analyses a posteriori suggérant systématiquement un bénéfice accru lorsque les taux de 25-OH-D étaient maintenus au-dessus de 40 ng/mL.
Références :
Manson JE, et al. Suppléments en vitamine D et prévention du cancer et des maladies cardiovasculaires (VITAL). N Engl J Med. 2019 ; 380(1) : 33-44.
Scragg R, et al. Effet d'une supplémentation mensuelle en vitamine D à forte dose sur les maladies cardiovasculaires dans l'essai ViDA. JAMA Cardiol. 2017 ; 2(6) : 608-16.
Essai TARGET-D. Supplémentation ajustée en vitamine D et résultats cardiovasculaires. 2024.

La médecine de la longévité surveille les deux extrémités de la fourchette de ferritine. Un taux de ferritine chroniquement élevé — même s'il se situe dans la limite supérieure de la « normale » conventionnelle — est associé au stress oxydatif, à la surcharge en fer, à la stéatose hépatique non alcoolique et au risque cardiovasculaire.
Données issues de la UK Biobank et d'une cohorte prospective : un taux de ferritine sérique situé dans la partie supérieure de la fourchette normale (> 200 ng/mL chez les hommes) a été associé à un risque accru de maladie hépatique, de syndrome métabolique, d'événements cardiovasculaires et de mortalité toutes causes confondues — indépendamment de la CRP —, ce qui suggère qu'une véritable surcharge en fer, plutôt qu'une élévation inflammatoire de la ferritine, serait en cause.
Références :
Ellervik C, Mandrup-Poulsen T, Andersen HU, et al. Saturation élevée de la transferrine et risque de diabète : trois études menées auprès de la population. Diabetes Care. 2011 ; 34(10) : 2256-2258. doi:10.2337/dc11-0416
Ellervik C, Marott JL, Tybjærg-Hansen A, Schnohr P, Nordestgaard BG. Mortalité totale et par cause spécifique associée à des concentrations de ferritine modérément et fortement élevées : étude sur la population générale et méta-analyse. Clin Chem. 2014 ; 60(11) : 1419-1428. doi:10.1373/clinchem.2014.229013
Mainous AG 3e et al. Un taux élevé de ferritine sérique est associé à un risque accru de diabète de type 2. J Am Board Fam Med. 2005 ; 18(3) : 174-81.
Kadoglou NPE, Biddulph JP, Rafnsson SB, Trivella M, Nihoyannopoulos P, Demakakos P. Association entre la ferritine et la mortalité cardiovasculaire et toutes causes confondues chez les personnes vivant en milieu communautaire : l'étude longitudinale anglaise sur le vieillissement. PLOS ONE. 2017 ; 12(6) : e0178994. doi:10.1371/journal.pone.0178994
† Les données d'observation concernant l'homocystéine sont solides ; les données issues d'essais cliniques randomisés sont faibles. Voir la section 3 pour plus de précisions.
MISES EN GARDE CLINIQUES IMPORTANTES
Plusieurs de ces marqueurs présentent une relation en forme de J ou de U avec la mortalité (HbA1c, acide urique, IGF-1, TSH) — ce qui signifie que tant les valeurs très élevées que les valeurs très basses comportent un risque. L'objectif est l'optimisation physiologique, et non la maximisation ou la minimisation d'un chiffre pris isolément.
Dans le domaine de la longévité, on distingue de plus en plus clairement l'association épidémiologique d'un biomarqueur avec la longévité et le bénéfice, étayé par des essais cliniques randomisés, d'une modification pharmacologique de ce biomarqueur. Pour certains marqueurs (homocystéine, HbA1c chez les diabétiques confirmés), ces deux aspects divergent considérablement. Dans la mesure du possible, il convient de viser des valeurs optimales par le biais d'une modification du mode de vie — alimentation, activité physique, sommeil et santé métabolique — plutôt que par le seul recours à des médicaments ou à des compléments alimentaires.
Le présent document reflète l'état des connaissances scientifiques à la période 2024-2025. Les valeurs de référence et les seuils thérapeutiques constituent des domaines en constante évolution ; les cliniciens doivent donc tenir compte du contexte individuel de chaque patient lorsqu'ils appliquent les valeurs présentées ici.