L'ApoB è la proteina principale presente su ogni particella di lipoproteina aterogena (LDL, VLDL, IDL, Lp(a)) — una particella, una molecola di ApoB. Questo la rende un indicatore diretto del numero di particelle, che dal punto di vista meccanicistico è più informativo rispetto alla sola concentrazione di colesterolo LDL.
The 2024 National Lipid Association Expert Consensus proposed stratified ApoB targets: <90 mg/dL for intermediate-risk, <70 mg/dL for high-risk, and <60 mg/dL for very high-risk patients — thresholds consistent with epidemiological data and treatment effects observed in lipid-lowering trials. In a 2024 analysis of over 500,000 UK Biobank participants, when LDL-C and ApoB were discordant, cardiovascular risk followed ApoB — not LDL-C. Elevated ApoB was also independently associated with increased Alzheimer's disease risk.
Riferimenti:
Handelsman Y, et al. Dichiarazione di consenso dell'Associazione Americana di Endocrinologia Clinica sulla gestione della dislipidemia. Endocr Pract. 2024.
Ibanez B, et al. Meta-analisi sul colesterolo LDL e l'aterosclerosi in soggetti a rischio ottimale. J Am Coll Cardiol. 2021.

L'allontanamento del settore della longevità dai valori target standard per il colesterolo LDL è in parte dovuto a un cambiamento nell'oggetto della misurazione — ora incentrata sul numero di particelle (ApoB) — e in parte a un abbassamento della soglia assoluta. Una meta-analisi fondamentale ha dimostrato che, anche in soggetti con tutti i fattori di rischio cardiovascolare entro i valori ottimali, esisteva una correlazione significativa tra la concentrazione di colesterolo LDL e la presenza di aterosclerosi.
Ibanez et al. (2021): Nei soggetti con valori ottimali per tutti i fattori di rischio cardiovascolare, è emersa una correlazione significativa tra la concentrazione di colesterolo LDL e l'aterosclerosi subclinica, il che suggerisce che non esista un livello di colesterolo LDL realmente sicuro dal punto di vista della formazione delle placche.
Riferimenti:
Ibanez B, et al. Aterosclerosi subclinica e colesterolo LDL in soggetti a rischio ottimale. J Am Coll Cardiol. 2021;77(24):3031–3041.
Ridker PM, et al. La rosuvastatina nella prevenzione degli eventi vascolari in uomini e donne con livelli elevati di proteina C-reattiva (JUPITER). N Engl J Med. 2008;359(21):2195–207.

A differenza di tutti gli altri biomarcatori citati in questo articolo, l'Lp(a) non può essere modificato dallo stile di vita. I livelli di Lp(a) sono determinati geneticamente per circa il 70-90% e rimangono stabili per tutta la vita, rendendo l'Lp(a) elevato un fattore di rischio cardiovascolare permanente. Nel campo della longevità, viene considerato un test fondamentale da eseguire una sola volta, che ridefinisce lifetime e giustifica una gestione più aggressiva di tutti gli altri fattori modificabili.
Studio sulla popolazione generale di Copenaghen (randomizzazione mendeliana, n=40.486): livelli geneticamente elevati di Lp(a) sono stati associati a un aumento del 22% del rischio di infarto miocardico per ogni raddoppio dei livelli di Lp(a).
Meta-analisi a livello di partecipante di 6 studi clinici controllati con placebo sulle statine: l’Lp(a) e l’LDL-C predicono il rischio di ASCVD in modo indipendente e additivo — il che significa che livelli elevati di Lp(a) comportano un rischio residuo significativo anche nei pazienti con LDL-C ben controllato.
The EAS 2022 consensus: the association between Lp(a) and ASCVD outcomes is continuous. The clinical cutoffs of <30 mg/dL and >50 mg/dL are pragmatic rather than biological. An Lp(a) of 100 mg/dL approximately doubles ASCVD risk, with the absolute increase substantially greater in higher-baseline-risk individuals.
Terapia emergente: il pelacarsen (oligonucleotide antisenso) ha ridotto l'Lp(a) fino all'80% alla dose massima negli studi di fase 2, con il 98% dei pazienti che ha raggiunto livelli inferiori a 50 mg/dL. Lo studio di fase 3 Lp(a)HORIZON sugli esiti cardiovascolari è attualmente in corso.
L'aggiornamento mirato della NLA del 2024 raccomanda di misurare l'Lp(a) almeno una volta in ogni adulto — una posizione ora condivisa dall'EAS, dall'ACC/AHA e dall'ESC.
Riferimenti:
Nordestgaard BG, et al. La lipoproteina (a) come fattore di rischio cardiovascolare: situazione attuale. Eur Heart J. 2010;31(23):2844–53.
Tsimikas S, et al. Terapia antisenso mirata all'apolipoproteina (a): uno studio di fase 1 randomizzato, in doppio cieco e controllato con placebo. Lancet. 2015;386(10002):1472–83.
Ridker PM, et al. Lipoproteina (a), colesterolo LDL e hs-CRP ed esiti cardiovascolari a 30 anni nelle donne. N Engl J Med. 2024.
Handelsman Y, et al. Aggiornamento mirato 2024 della NLA. J Clin Lipidol. 2024.

L'HbA1c riflette il livello medio di zucchero nel sangue negli ultimi 2-3 mesi. Gli studi sui centenari mostrano costantemente valori di HbA1c inferiori al 6% per tutta la vita, con la mortalità per tutte le cause più bassa nelle popolazioni non diabetiche osservata nell'intervallo 5,0-5,6% (dati NHANES III). L'obiettivo ottimizzato per la longevità, compreso tra il 5,0 e il 5,4%, riflette queste evidenze. Nota: il limite inferiore del 5,0% è importante — i dati NHANES mostrano una relazione a forma di U nei non diabetici, con un HbA1c inferiore al 5,0% associato a un aumento della mortalità, che riflette probabilmente anemia, malattie epatiche o altre patologie confondenti piuttosto che un controllo metabolico benefico.
Set di dati NHANES III: i partecipanti senza diabete e con HbA1c compresa tra il 5,0% e il 5,6% rappresentavano la categoria di riferimento con la mortalità per tutte le cause più bassa. Il diabete non diagnosticato (HbA1c >6,5%) comportava un rischio di mortalità per tutte le cause 1,3 volte maggiore.
Coorte di centenari (Catalogna): i biomarcatori legati al metabolismo del glucosio — tra cui l'HbA1c e la glicemia a digiuno — hanno avuto un impatto negativo significativo sulla probabilità di arrivare a un'età molto avanzata quando si trovavano nei quintili più alti.
Una sfumatura importante: lo studio clinico randomizzato (RCT) ACCORD ha rilevato che un abbassamento farmacologico intensivo dell'HbA1c al di sotto del 6,5% nei pazienti con diabete di tipo 2 conclamato aumentava la mortalità — attribuibile all'ipoglicemia causata da una terapia farmacologica aggressiva. L'obiettivo per una vita più lunga è un livello naturalmente basso di HbA1c ottenuto attraverso la salute metabolica, non la soppressione farmacologica nei pazienti fragili o diabetici.
Riferimenti:
Selvin E, et al. Emoglobina glicata, diabete e rischio cardiovascolare negli adulti non diabetici. N Engl J Med. 2010;362(9):800–11.
Gruppo di studio ACCORD. Effetti di una terapia ipoglicemizzante intensiva nel diabete di tipo 2. N Engl J Med. 2008;358(24):2545–59.
Ponjoan A, et al. Profilo dei biomarcatori dei centenari in una coorte basata sulla popolazione. GeroScience. 2023.
Carson AP, Fox CS, McGuire DK, et al. Bassi livelli di emoglobina A1c e rischio di mortalità per tutte le cause negli adulti statunitensi non diabetici. Circ Cardiovasc Qual Outcomes. 2010;3(6):661-667

Gli intervalli di riferimento standard di laboratorio per l'insulina a digiuno sono particolarmente ampi. Gli attuali intervalli di riferimento non definiscono l'iperinsulinemia finché l'insulina a digiuno non supera i 24,9 µIU/mL — un valore da tre a cinque volte superiore a quello che i medici specializzati in longevità considerano ottimale. Un livello elevato di insulina a digiuno è un segnale precoce di insulino-resistenza rispetto all'HbA1c, e spesso si manifesta anni prima che la disregolazione glicemica diventi evidente.
Meta-analisi prospettica (Zhang et al., Bioscience Reports, 2017): ogni aumento di un'unità dell'insulina a digiuno entro i valori normali era associato a un aumento del 5% del rischio cardiovascolare. Chi presentava un'insulina a digiuno inferiore a 5 µIU/mL mostrava una mortalità cardiovascolare e per tutte le cause significativamente più bassa. Xun et al. hanno dimostrato che ogni aumento di 50 pmol/L dell'insulina a digiuno era associato a un aumento del 25% del rischio di ipertensione e a un aumento del 16% del rischio di CHD.
Riferimenti:
Zhang X, et al. Insulina a digiuno, insulino-resistenza e rischio di ipertensione nella popolazione generale. Bioscience Reports. 2017;37(5):BSR20160343.
Sung KCC, Seo MHH, Rhee EJJ, Wilson AM. L'insulina a digiuno elevata predice l'insorgenza futura della sindrome metabolica: uno studio di follow-up di 5 anni. Cardiovasc Diabetol. 2011;10(1):108. doi:10.1186/1475-2840-10-108
Xun P, Wu Y, He Q, He K. Concentrazioni di insulina a digiuno e incidenza di ipertensione, ictus e cardiopatia coronarica: una meta-analisi di studi prospettici di coorte123. The American Journal of Clinical Nutrition. 2013;98(6):1543-1554.

Sebbene la soglia clinica per il prediabete inizi a 100 mg/dL, i dati di coorti prospettiche mostrano che una glicemia a digiuno compresa tra 90 e 99 mg/dL è associata a un rischio cardiovascolare e metabolico progressivamente crescente rispetto a livelli inferiori a 90 mg/dL. Nel campo della longevità, questa fascia viene considerata un segnale di allarme precoce piuttosto che un risultato normale rassicurante.
Riferimenti:
Levitan EB, et al. L'iperglicemia non diabetica è un fattore di rischio per le malattie cardiovascolari? Arch Intern Med. 2004;164(19):2147–55.
Rijkelijkhuizen JM, et al. Valori soglia ottimali per la glicemia a digiuno e il rischio cardiovascolare associato. Diabetes Care. 2007;30(5):1167–72.
Bao C, Zhang D, Sun B, et al. Valori soglia ottimali della glicemia a digiuno per una strategia in due fasi nella stima della prevalenza e nello screening del diabete e del pre-diabete non diagnosticati a Harbin, in Cina. PLOS ONE. 2015;10(3):e0119510.
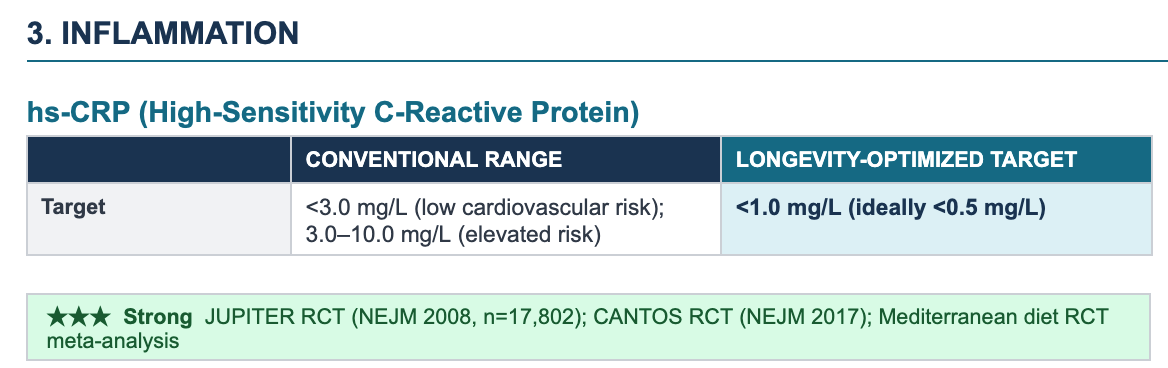
I dati chiave degli studi clinici randomizzati controllati (RCT) provengono dallo storico studio JUPITER: uno studio randomizzato e controllato con placebo condotto su 17.802 uomini e donne apparentemente sani, che ha dimostrato come la hs-CRP sia un indicatore di rischio cardiovascolare indipendente e utilizzabile a fini clinici anche nei pazienti con livelli normali di colesterolo LDL.
JUPITER within-trial dose-response analysis: participants who achieved hs-CRP below 1 mg/L on rosuvastatin saw a 79% reduction in cardiovascular events — substantially more than those who achieved LDL-C reduction alone, firmly establishing <1 mg/L as the longevity-optimized target.
Meta-analisi degli studi clinici randomizzati sulla dieta mediterranea: la dieta mediterranea ha ridotto la hs-CRP in media di 0,98 mg/L; una dieta ricca di fibre ha ridotto la hs-CRP del 28% — un effetto paragonabile a quello del trattamento con 20 mg al giorno di lovastatina.
Dati sui centenari (PMC 2025): la popolazione dei centenari presenta livelli plasmatici di CRP significativamente più bassi (0,9 ± 0,4 mg/L) rispetto agli anziani di età media (2,8 ± 1,6 mg/L), con differenze che persistono anche dopo aver tenuto conto delle comorbilità.
Riferimenti:
Ridker PM, et al. La rosuvastatina nella prevenzione degli eventi vascolari in uomini e donne con livelli elevati di proteina C-reattiva (JUPITER). N Engl J Med. 2008;359(21):2195–207.
Ridker PM, Danielson E, Fonseca FA, et al. Riduzione della proteina C-reattiva e del colesterolo LDL e dei tassi di eventi cardiovascolari dopo l’inizio della terapia con rosuvastatina: uno studio prospettico del trial JUPITER. The Lancet. 2009;373(9670):1175-1182. doi:10.1016/S0140-6736(09)60447-5
Ridker PM, et al. Terapia antinfiammatoria con canakinumab per la malattia aterosclerotica (CANTOS). N Engl J Med. 2017;377(12):1119–31.
Ridker PM, et al. Livelli di proteina C-reattiva ed esiti dopo la terapia con statine. N Engl J Med. 2005;352(1):20–8.
Keshani M, Rafiee S, Heidari H, Rouhani MH, Sharma M, Bagherniya M. La dieta mediterranea riduce l'infiammazione negli adulti: una revisione sistematica e una meta-analisi di studi randomizzati controllati. Nutr Rev. Pubblicato online il 10 novembre 2025:nuaf213. doi:10.1093/nutrit/nuaf213
Adibi S. Un quadro concettuale di salute digitale per l'ottimizzazione della longevità: un approccio incentrato sull'infiammazione che integra dati sul microbioma e sullo stile di vita — Una revisione e una proposta di piattaforma. Nutrients. 2026;18(2):231.

I dati prospettici associano costantemente livelli di omocisteina superiori a 9–10 µmol/L alla mortalità per malattie cardiovascolari e neurodegenerative. Tuttavia, le prove scientifiche relative all'omocisteina sono più complesse rispetto a quelle relative agli altri biomarcatori citati in questo articolo.
Nygård et al. (NEJM, 1997): nei pazienti con malattia coronarica confermata dall'angiografia, livelli di omocisteina compresi tra 9,0 e 14,9 µmol/L erano già associati a un rapporto di mortalità pari a 3,3 rispetto a livelli inferiori a 9 µmol/L — che saliva a 9,9 per livelli ≥20 µmol/L.
Meta-analisi PMC di 12 studi prospettici (n=23.623): confrontando le categorie con i livelli più alti e quelli più bassi di omocisteina, la mortalità per cardiopatia coronarica è aumentata del 66%, quella cardiovascolare del 68%, e ogni aumento di 5 µmol/L è stato associato a un aumento del 52% della mortalità per cardiopatia coronarica.
Avvertenza fondamentale sugli RCT: studi di riferimento — HOPE-2 (2006), NORVIT (2006) e VITATOPS (2010) — sono riusciti a ridurre i livelli plasmatici di omocisteina grazie all’integrazione con vitamine del gruppo B, ma non sono riusciti, in gran parte, a ridurre gli esiti cardiovascolari gravi, tra cui infarto miocardico, ictus o mortalità per tutte le cause. Una successiva meta-analisi di 19 RCT (n=47.921) ha rilevato che l'integrazione con vitamine del gruppo B ha ridotto significativamente il rischio di ictus, ma non di CVD, IM, CHD o mortalità per tutte le cause. Ciò non nega il valore dell'omocisteina come biomarcatore di rischio, ma mette in guardia dal presumere che la sola normalizzazione farmacologica migliori gli esiti.
Riferimenti:
Nygård O, et al. Livelli plasmatici di omocisteina e mortalità nei pazienti con malattia coronarica. N Engl J Med. 1997;337(4):230–6.
Lonn E, et al. Terapia per abbassare i livelli di omocisteina ed esiti nei pazienti ad alto rischio (HOPE-2). N Engl J Med. 2006;354(15):1567–77.
Clarke R, et al. Effetti della riduzione dei livelli di omocisteina con le vitamine del gruppo B sulle malattie cardiovascolari, sul cancro e sulla mortalità per cause specifiche: meta-analisi di 8 studi randomizzati. Arch Intern Med. 2010;170(18):1622–31.
Homocysteine Studies Collaboration. Omocisteina e rischio di cardiopatia ischemica e ictus: una meta-analisi. JAMA. 2002;288(16):2015-2022. doi:10.1001/jama.288.16.2015
Peng H et al. Livelli elevati di omocisteina e rischio di mortalità cardiovascolare e per tutte le cause: una meta-analisi di studi prospettici. J Zhejiang Univ Sci B. 2015;16(1):78-86.

L'IL-6 è la citochina pro-infiammatoria più studiata nel contesto dell'invecchiamento biologico ("inflammaging"). Gli intervalli di riferimento standard dei laboratori sono derivati dalla popolazione e non riflettono i livelli associati a risultati ottimali in termini di longevità.
Centenarian cohort data (PMC 2025): centenarians demonstrate significantly reduced plasma IL-6 (1.4 ± 0.6 pg/mL) compared to average-aging elderly individuals (3.2 ± 1.8 pg/mL, p<0.001). These differences persist after controlling for comorbidities, suggesting low inflammatory status is a characteristic feature of exceptional longevity.
Tylutka et al., Frontiers in Immunology (2024, PRISMA meta-analysis): the overall IL-6 concentration was significantly higher in patients with age-related diseases compared to controls (SMD 0.16, p<0.001). IL-6 demonstrated diagnostic utility as an independent predictor of age-related morbidity and mortality in elderly adults.
Randomizzazione mendeliana (npj Genomic Medicine, 2019): la via di segnalazione dell'IL-6 ha mostrato associazioni causali inverse con la fibrillazione atriale, l'ictus, la malattia coronarica e l'aneurisma dell'aorta addominale — ed è risultata associata positivamente all'età dei genitori al momento del decesso (indicatore di longevità).
Riferimenti:
Tylutka A, et al. Livelli di IL-6, TNF e IL-1β e malattie legate all'età: una revisione sistematica e una meta-analisi. Front Immunol. 2024;15:1330386.
Collaborazione (dati sui centenari). Un quadro concettuale di salute digitale per l'ottimizzazione della longevità. PMC 2025.
Georgakis MK, et al. La segnalazione dell'IL-6 nelle malattie cardiovascolari, nei disturbi immunitari e nella longevità. npj Genomic Medicine. 2019.
Adibi S. Un quadro concettuale di salute digitale per l'ottimizzazione della longevità: un approccio incentrato sull'infiammazione che integra dati sul microbioma e sullo stile di vita — Una revisione e una proposta di piattaforma. Nutrients. 2026;18(2):231.

L'IGF-1 è più complesso della maggior parte dei biomarcatori: un livello più alto non è affatto sinonimo di meglio. La relazione con la longevità ha un andamento a U: sia i livelli molto bassi che quelli molto alti comportano un rischio maggiore, mentre i livelli intermedi sono associati alla mortalità più bassa.
Longo et al., Aging Cell (2022) — meta-analisi di 19 studi prospettici di coorte (n=30.876): l'analisi dose-risposta ha rivelato una relazione a forma di U tra l'IGF-1 e l'HR della mortalità per tutte le cause. L'intervallo 120–160 ng/mL era associato alla mortalità più bassa. Il confronto tra livelli bassi e medi di IGF-1 ha mostrato un aumento significativo della mortalità per tutte le cause (HR=1,33, IC al 95%: 1,14–1,57); anche il confronto tra livelli alti e medi ha mostrato una mortalità elevata (HR=1,23, IC al 95%: 1,06–1,44).
EPIC-Heidelberg (Mukama et al., J Clin Endocrinol Metab, 2023, studio prospettico basato sulla popolazione): livelli più elevati di IGF-1 hanno mostrato un'associazione diretta con il rischio di cancro al seno (HR 1,25) e di cancro alla prostata (HR 1,31). Sia i livelli più bassi che quelli più alti di IGF-1 erano associati a un aumento del rischio di morte per cancro, malattie cardiovascolari e tutte le cause — confermando la relazione a forma di U in un’ampia popolazione europea.
In pratica: punta a mantenere l'IGF-1 entro un intervallo fisiologico medio — cosa che di solito si ottiene con un apporto proteico adeguato ma non eccessivo, un'attività fisica regolare e un sonno sano — piuttosto che cercare un'ottimizzazione farmacologica dell'asse GH/IGF-1.
Riferimenti:
Rahmani J, et al. Associazione tra i livelli di IGF-1 e la mortalità per tutte le cause: una meta-analisi. Aging Cell. 2022;21(2):e13540.
Mukama T, et al. IGF-1 e rischio di morbilità e mortalità per cancro, malattie cardiovascolari e tutte le cause nello studio EPIC-Heidelberg. J Clin Endocrinol Metab. 2023;108(10):e1092–e1105.

Le prove più solide provengono da una meta-analisi IPD pubblicata nel 2023 su *Lancet Diabetes & Endocrinology* — uno dei più grandi studi sulla funzione tiroidea mai condotti — che si è espressamente prefissata di definire gli intervalli ottimali di TSH e FT4 sulla base degli esiti clinici piuttosto che dei percentili statistici della popolazione.
Xu et al., Lancet Diabetes & Endocrinology (2023), n=134.346, follow-up medio 11,5 anni: sono state individuate associazioni non lineari per il TSH, con i percentili 60–80 (mediana 1,90–2,90 mIU/L) associati al rischio più basso di malattie cardiovascolari e mortalità. L'FT4 ha mostrato un'associazione a forma di J con il 20°-40° percentile (mediana 13,5–14,8 pmol/L) che indicava il rischio più basso. L'FT4 nell'80°-100° percentile era associato a un aumento di 1,34 volte della mortalità per tutte le cause e a un aumento di 1,57 volte della mortalità per CVD rispetto all'intervallo ottimale.
Interpretazione: Il valore di TSH ottimale per la longevità non si trova né nella fascia bassa (associata a ipertiroidismo subclinico e a un rischio elevato di malattie cardiovascolari e mortalità) né al limite superiore convenzionale di 4,0 mIU/L. È proprio nell'intervallo di TSH compreso tra 1,9 e 2,9 mIU/L — che la maggior parte dei medici considererebbe attualmente nella norma — che il rischio di mortalità è più basso. Soprattutto per le persone anziane, un TSH nella parte alta della norma potrebbe essere un meccanismo di adattamento piuttosto che un segno di patologia.
Riferimenti:
Xu Y, et al. Intervalli ottimali di funzionalità tiroidea definiti in base al rischio di malattie cardiovascolari e mortalità: revisione sistematica e meta-analisi basata sui dati individuali dei partecipanti. Lancet Diabetes Endocrinol. 2023;11(10):743–754. PMID: 37696273.
Razvi S, et al. L'effetto benefico della L-tiroxina sui fattori di rischio cardiovascolare, sulla funzione endoteliale e sulla qualità della vita nell'ipotiroidismo subclinico. J Clin Endocrinol Metab. 2007;92(5):1715–23.

I laboratori standard segnalano un livello "basso" di testosterone solo quando si raggiunge il limite minimo della popolazione: una soglia statistica, non ottimizzata per la salute. La medicina della longevità è meno interessata a evitare i livelli "bassi" e più concentrata sul mantenimento di livelli associati alla salute metabolica, alla conservazione della massa muscolare, alla sensibilità all'insulina e alla protezione cognitiva — in genere nella fascia medio-alta per l'età.
The Testosterone Trials (TTrials, NEJM 2016): in men 65+ with low testosterone (<275 ng/dL), testosterone treatment improved sexual function, physical function, and quality of life, with additional signals for bone density and anemia. Metabolic benefits were observed at levels in the mid-normal range.
Riferimenti:
Snyder PJ, et al. Effetti del trattamento con testosterone negli uomini anziani (TTrials). N Engl J Med. 2016;374(7):611–24.
Araujo AB, Dixon JM, Suarez EA, Murad MH, Guey LT, Wittert GA. Revisione clinica: Testosterone endogeno e mortalità negli uomini: una revisione sistematica e una meta-analisi. J Clin Endocrinol Metab. 2011;96(10):3007-3019. doi:10.1210/jc.2011-1137

La medicina convenzionale interviene solo quando l'eGFR è inferiore a 60 mL/min/1,73 m². Il settore della longevità riconosce che anche un declino subclinico compreso tra 60 e 89 aumenta significativamente il rischio di mortalità cardiovascolare e per tutte le cause, rendendo un valore >90 un obiettivo da perseguire attivamente piuttosto che un semplice parametro di riferimento irrilevante.
Consorzio sulla prognosi della CKD (Lancet, 2010, n => 1,1 milioni): è emersa un'associazione continua, indipendente e graduale sia tra la riduzione dell'eGFR sia tra l'aumento dell'albuminuria e la mortalità per tutte le cause, la mortalità cardiovascolare e l'insufficienza renale — con un rischio in eccesso significativo che inizia già al di sotto di un eGFR di 75 mL/min/1,73 m², non solo alla soglia della CKD di 60.
Riferimenti:
Matsushita K, et al. Associazione tra la velocità di filtrazione glomerulare stimata e l'albuminuria con la mortalità per tutte le cause e quella cardiovascolare in coorti della popolazione generale: una meta-analisi collaborativa. Lancet. 2010;375(9731):2073–81.

I dati degli studi clinici sulla vitamina D sono stati storicamente contrastanti, ma le prove a sostegno del valore target di 40–60 ng/mL si sono notevolmente rafforzate grazie a recenti studi randomizzati controllati.
Studio RCT TARGET-D (2024): nei pazienti ad alto rischio, l'integrazione di vitamina D regolata per raggiungere livelli superiori a 40 ng/mL ha ridotto significativamente il rischio di recidiva di infarto — uno dei primi studi RCT a dimostrare un beneficio cardiovascolare legato specificamente al raggiungimento di un livello target superiore a 40 ng/mL.
Studio VITAL RCT (NEJM, 2019, n=25.871): sebbene gli endpoint primari non abbiano registrato una riduzione significativa, le analisi prestabilite hanno evidenziato una riduzione significativa della mortalità per cancro nei partecipanti con un BMI basso — mentre le analisi post hoc hanno costantemente indicato un beneficio maggiore quando i livelli di 25-OH-D venivano mantenuti al di sopra dei 40 ng/mL.
Riferimenti:
Manson JE, et al. Integratori di vitamina D e prevenzione del cancro e delle malattie cardiovascolari (VITAL). N Engl J Med. 2019;380(1):33–44.
Scragg R, et al. Effetto dell'integrazione mensile ad alto dosaggio di vitamina D sulle malattie cardiovascolari nello studio ViDA. JAMA Cardiol. 2017;2(6):608–16.
Studio TARGET-D. Supplementazione titolata di vitamina D ed esiti cardiovascolari. 2024.

La medicina della longevità tiene d'occhio entrambi i limiti dell'intervallo di ferritina. Livelli cronicamente elevati di ferritina — anche se rientrano nel limite superiore convenzionalmente considerato "normale" — sono associati a stress ossidativo, sovraccarico di ferro, steatosi epatica non alcolica e rischio cardiovascolare.
Dati della UK Biobank e di coorti prospettiche: livelli di ferritina sierica nella fascia superiore della norma (>200 ng/mL negli uomini) sono risultati associati a un aumento del rischio di malattie epatiche, sindrome metabolica, eventi cardiovascolari e mortalità per tutte le cause — indipendentemente dalla CRP — suggerendo che il fattore determinante sia un vero e proprio sovraccarico di ferro piuttosto che un aumento infiammatorio della ferritina.
Riferimenti:
Ellervik C, Mandrup-Poulsen T, Andersen HU, et al. Aumento della saturazione della transferrina e rischio di diabete: tre studi basati sulla popolazione. Diabetes Care. 2011;34(10):2256-2258. doi:10.2337/dc11-0416
Ellervik C, Marott JL, Tybjærg-Hansen A, Schnohr P, Nordestgaard BG. Mortalità totale e per cause specifiche in presenza di concentrazioni di ferritina moderatamente e marcatamente elevate: studio sulla popolazione generale e meta-analisi. Clin Chem. 2014;60(11):1419-1428. doi:10.1373/clinchem.2014.229013
Mainous AG 3rd, et al. Livelli elevati di ferritina sierica sono associati a un aumento del rischio di diabete di tipo 2. J Am Board Fam Med. 2005;18(3):174–81.
Kadoglou NPE, Biddulph JP, Rafnsson SB, Trivella M, Nihoyannopoulos P, Demakakos P. L'associazione tra ferritina e mortalità cardiovascolare e per tutte le cause nella popolazione residente: lo studio longitudinale inglese sull'invecchiamento. PLOS ONE. 2017;12(6):e0178994. doi:10.1371/journal.pone.0178994
† Il segnale osservazionale relativo all'omocisteina è forte; le prove derivanti dagli studi clinici randomizzati controllati (RCT) sono deboli. Vedi la Sezione 3 per ulteriori dettagli.
AVVERTENZE CLINICHE IMPORTANTI
Molti di questi indicatori presentano una relazione a forma di J o di U con la mortalità (HbA1c, acido urico, IGF-1, TSH), il che significa che sia i valori molto alti che quelli molto bassi comportano un rischio. L'obiettivo è l'ottimizzazione fisiologica, non la massimizzazione o la minimizzazione di un valore preso isolatamente.
Nel campo della longevità si tende sempre più a distinguere tra l'associazione epidemiologica di un biomarcatore con la longevità e il beneficio, dimostrato da studi clinici randomizzati controllati (RCT), derivante dall'alterazione farmacologica di quel biomarcatore. Per alcuni marcatori (omocisteina, HbA1c nei pazienti diabetici conclamati), questi due aspetti divergono in modo significativo. Ove possibile, è preferibile cercare di raggiungere i valori ottimali attraverso modifiche dello stile di vita — alimentazione, esercizio fisico, sonno e salute metabolica — piuttosto che ricorrere esclusivamente alla terapia farmacologica o all'uso di integratori.
Questo documento riflette le evidenze scientifiche disponibili al 2024–2025. Gli intervalli di riferimento e le soglie terapeutiche sono ambiti in continua evoluzione; i medici dovrebbero tenere conto delle condizioni specifiche di ciascun paziente nel valutare tutti i valori di riferimento qui riportati.