ApoB ist das Hauptprotein, das auf jedem atherogenen Lipoproteinpartikel (LDL, VLDL, IDL, Lp(a)) vorkommt – ein Partikel, ein ApoB-Molekül. Damit handelt es sich um eine direkte Partikelzählung, die aus mechanistischer Sicht aussagekräftiger ist als die LDL-Cholesterinkonzentration allein.
The 2024 National Lipid Association Expert Consensus proposed stratified ApoB targets: <90 mg/dL for intermediate-risk, <70 mg/dL for high-risk, and <60 mg/dL for very high-risk patients — thresholds consistent with epidemiological data and treatment effects observed in lipid-lowering trials. In a 2024 analysis of over 500,000 UK Biobank participants, when LDL-C and ApoB were discordant, cardiovascular risk followed ApoB — not LDL-C. Elevated ApoB was also independently associated with increased Alzheimer's disease risk.
Quellen:
Handelsman Y. et al. Konsenserklärung der American Association of Clinical Endocrinology zur Behandlung von Dyslipidämie. Endocr Pract. 2024.
Ibanez B. et al. Metaanalyse zu LDL-C und Atherosklerose bei Personen mit optimalem Risiko. J Am Coll Cardiol. 2021.

Die Abkehr des Bereichs der Langlebigkeit von den üblichen LDL-C-Zielwerten ist zum einen auf eine Verlagerung des Messfokus – hin zur Partikelanzahl (ApoB) – und zum anderen auf eine Senkung des absoluten Schwellenwerts zurückzuführen. Eine wichtige Metaanalyse hat gezeigt, dass selbst bei Personen, bei denen alle kardiovaskulären Risikofaktoren im optimalen Bereich lagen, ein signifikanter Zusammenhang zwischen der LDL-C-Konzentration und dem Vorliegen von Atherosklerose bestand.
Ibanez et al. (2021): Bei Personen mit optimalen Werten für alle kardiovaskulären Risikofaktoren bestand ein signifikanter Zusammenhang zwischen der LDL-C-Konzentration und subklinischer Atherosklerose – was darauf hindeutet, dass es aus Sicht der Plaquebildung keinen wirklich sicheren LDL-C-Spiegel gibt.
Quellen:
Ibanez B. et al. Subklinische Atherosklerose und LDL-C bei Personen mit optimalem Risiko. J Am Coll Cardiol. 2021;77(24):3031–3041.
Ridker PM et al. Rosuvastatin zur Vorbeugung vaskulärer Ereignisse bei Männern und Frauen mit erhöhtem C-reaktivem Protein (JUPITER). N Engl J Med. 2008;359(21):2195–207.

Im Gegensatz zu allen anderen Biomarkern in diesem Artikel lässt sich Lp(a) nicht durch den Lebensstil beeinflussen. Der Lp(a)-Spiegel ist zu etwa 70–90 % genetisch bedingt und bleibt ein Leben lang stabil – was einen erhöhten Lp(a)-Spiegel zu einem lebenslangen kardiovaskulären Risikofaktor macht. Im Bereich der Langlebigkeitsforschung wird er als grundlegender einmaliger Test betrachtet, der lifetime neu definiert und eine aggressivere Behandlung aller anderen beeinflussbaren Faktoren rechtfertigt.
Kopenhagener Bevölkerungsstudie (Mendelsche Randomisierung, n = 40.486): Ein genetisch bedingter erhöhter Lp(a)-Spiegel war mit einem um 22 % erhöhten Risiko für einen Herzinfarkt pro Verdopplung des Lp(a)-Spiegels verbunden.
Meta-Analyse auf Teilnehmerebene von 6 placebokontrollierten Statin-Studien: Lp(a) und LDL-C sagen das ASCVD-Risiko unabhängig voneinander und additiv voraus – das heißt, ein erhöhter Lp(a)-Wert birgt selbst bei Patienten mit gut kontrolliertem LDL-C ein signifikantes Restrisiko.
The EAS 2022 consensus: the association between Lp(a) and ASCVD outcomes is continuous. The clinical cutoffs of <30 mg/dL and >50 mg/dL are pragmatic rather than biological. An Lp(a) of 100 mg/dL approximately doubles ASCVD risk, with the absolute increase substantially greater in higher-baseline-risk individuals.
Eine neue Therapie: Pelacarsen (Antisense-Oligonukleotid) senkte in Phase-2-Studien bei der höchsten Dosis den Lp(a)-Spiegel um bis zu 80 %, wobei 98 % der Patienten Werte unter 50 mg/dl erreichten. Die Phase-3-Studie „Lp(a)HORIZON“ zu kardiovaskulären Endpunkten läuft derzeit.
Die aktualisierte Empfehlung der NLA aus dem Jahr 2024 sieht vor, bei jedem Erwachsenen mindestens einmal den Lp(a)-Wert zu messen – eine Position, die mittlerweile auch von der EAS, dem ACC/AHA und der ESC geteilt wird.
Quellen:
Nordestgaard BG et al. Lipoprotein(a) als kardiovaskulärer Risikofaktor: aktueller Stand. Eur Heart J. 2010;31(23):2844–53.
Tsimikas S. et al. Antisense-Therapie gegen Apolipoprotein(a): eine randomisierte, doppelblinde, placebokontrollierte Phase-1-Studie. Lancet. 2015;386(10002):1472–83.
Ridker PM et al. Lipoprotein(a), LDL-C und hs-CRP sowie kardiovaskuläre 30-Jahres-Ergebnisse bei Frauen. N Engl J Med. 2024.
Handelsman Y. et al. NLA-Fokus-Update 2024. J Clin Lipidol. 2024.

HbA1c spiegelt den durchschnittlichen Blutzuckerspiegel der letzten 2–3 Monate wider. Studien an Hundertjährigen zeigen durchweg einen HbA1c-Wert unter 6 % über das gesamte Leben hinweg, wobei die niedrigste Gesamtmortalität in nicht-diabetischen Bevölkerungsgruppen im Bereich von 5,0–5,6 % beobachtet wurde (NHANES-III-Daten). Der auf Langlebigkeit optimierte Zielwert von 5,0–5,4 % spiegelt diese Erkenntnisse wider. Hinweis: Die Untergrenze von 5,0 % ist wichtig – NHANES-Daten zeigen bei Nicht-Diabetikern eine U-förmige Beziehung, wobei ein HbA1c-Wert unter 5,0 % mit einer erhöhten Sterblichkeit verbunden ist, was wahrscheinlich eher auf Anämie, Lebererkrankungen oder andere Störfaktoren zurückzuführen ist als auf eine vorteilhafte Stoffwechselkontrolle.
NHANES-III-Datensatz: Teilnehmer ohne Diabetes und mit einem HbA1c-Wert im Bereich von 5,0–5,6 % bildeten die Referenzgruppe mit der niedrigsten Gesamtmortalität. Nicht diagnostizierter Diabetes (HbA1c > 6,5 %) war mit einem 1,3-fach höheren Risiko für die Gesamtmortalität verbunden.
Kohorte von Hundertjährigen (Katalonien): Biomarker im Zusammenhang mit dem Glukosestoffwechsel – darunter HbA1c und Nüchternblutzucker – hatten einen signifikanten negativen Einfluss auf die Wahrscheinlichkeit, ein extrem hohes Alter zu erreichen, wenn sie im obersten Quintil lagen.
Wichtige Nuance: Die ACCORD-RCT ergab, dass eine intensive medikamentöse Senkung des HbA1c-Werts unter 6,5 % bei etablierten Typ-2-Diabetikern die Sterblichkeit erhöhte – was auf Hypoglykämien infolge einer aggressiven medikamentösen Therapie zurückgeführt wurde. Das Ziel für ein langes Leben ist ein auf natürliche Weise niedriger HbA1c-Wert durch Stoffwechselgesundheit, nicht durch medikamentöse Unterdrückung bei gebrechlichen oder diabetischen Patienten.
Quellen:
Selvin E. et al. Glykiertes Hämoglobin, Diabetes und kardiovaskuläres Risiko bei nicht-diabetischen Erwachsenen. N Engl J Med. 2010;362(9):800–11.
ACCORD-Studiengruppe. Auswirkungen einer intensiven Blutzuckersenkung bei Typ-2-Diabetes. N Engl J Med. 2008;358(24):2545–59.
Ponjoan A. et al. Biomarkerprofil von Hundertjährigen in einer bevölkerungsbasierten Kohorte. GeroScience. 2023.
Carson AP, Fox CS, McGuire DK et al. Niedrige HbA1c-Werte und das Risiko der Gesamtmortalität bei Erwachsenen in den USA ohne Diabetes. Circ Cardiovasc Qual Outcomes. 2010;3(6):661-667

Die gängigen Laborreferenzbereiche für Nüchterninsulin sind bemerkenswert großzügig bemessen. Nach den heutigen Laborreferenzbereichen liegt eine Hyperinsulinämie erst dann vor, wenn der Nüchterninsulinspiegel über 24,9 µIU/ml steigt – das ist drei- bis fünfmal höher als der Wert, den auf Langlebigkeit spezialisierte Ärzte als optimal ansehen. Ein erhöhter Nüchterninsulinspiegel ist ein früheres Anzeichen für Insulinresistenz als HbA1c und tritt oft schon Jahre vor dem Auftreten einer offensichtlichen Glukoseregulationsstörung auf.
Prospektive Metaanalyse (Zhang et al., Bioscience Reports, 2017): Jeder Anstieg des Nüchterninsulinspiegels um eine Einheit innerhalb des Normalbereichs war mit einem Anstieg des kardiovaskulären Risikos um 5 % verbunden. Bei Personen mit einem Nüchterninsulinspiegel unter 5 µIU/ml war die kardiovaskuläre Mortalität sowie die Gesamtmortalität signifikant niedriger. Xun et al. zeigten, dass jeder Anstieg des Nüchterninsulinspiegels um 50 pmol/L mit einem um 25 % erhöhten Risiko für Bluthochdruck und einem um 16 % erhöhten Risiko für eine koronare Herzkrankheit (KHK) verbunden war.
Quellen:
Zhang X. et al. Nüchterninsulin, Insulinresistenz und das Risiko für Bluthochdruck in der Allgemeinbevölkerung. Bioscience Reports. 2017;37(5):BSR20160343.
Sung KCC, Seo MHH, Rhee EJJ, Wilson AM. Ein erhöhter Nüchterninsulinspiegel sagt das künftige Auftreten des metabolischen Syndroms voraus: eine 5-Jahres-Folgestudie. Cardiovasc Diabetol. 2011;10(1):108. doi:10.1186/1475-2840-10-108
Xun P, Wu Y, He Q, He K. Nüchterninsulinspiegel und das Auftreten von Bluthochdruck, Schlaganfall und koronarer Herzkrankheit: eine Metaanalyse prospektiver Kohortenstudien123. The American Journal of Clinical Nutrition. 2013;98(6):1543-1554.

Zwar beginnt die klinische Schwelle für Prädiabetes bei 100 mg/dl, doch zeigen prospektive Kohortendaten, dass ein Nüchternblutzucker im Bereich von 90–99 mg/dl im Vergleich zu Werten unter 90 mg/dl mit einem zunehmend höheren kardiovaskulären und metabolischen Risiko verbunden ist. In der Langlebigkeitsforschung wird dieser Bereich eher als Frühwarnsignal denn als beruhigendes normales Ergebnis betrachtet.
Quellen:
Levitan EB et al. Ist eine nicht-diabetische Hyperglykämie ein Risikofaktor für Herz-Kreislauf-Erkrankungen? Arch Intern Med. 2004;164(19):2147–55.
Rijkelijkhuizen JM et al. Optimale Grenzwerte für den Nüchternblutzucker und das damit verbundene kardiovaskuläre Risiko. Diabetes Care. 2007;30(5):1167–72.
Bao C, Zhang D, Sun B, et al. Optimale Grenzwerte für den Nüchternplasmaglukosespiegel bei einer Zwei-Stufen-Strategie zur Schätzung der Prävalenz und zum Screening auf nicht diagnostizierten Diabetes und Prädiabetes in Harbin, China. PLOS ONE. 2015;10(3):e0119510.
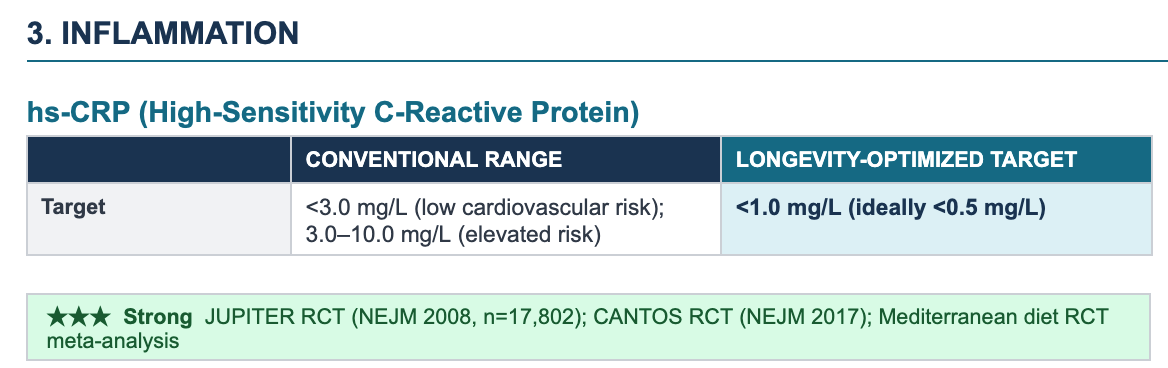
Die entscheidenden Erkenntnisse aus randomisierten kontrollierten Studien stammen aus der wegweisenden JUPITER-Studie: einer randomisierten, placebokontrollierten Studie mit 17.802 scheinbar gesunden Männern und Frauen, die den hochsensitiven C-reaktiven Protein (hs-CRP) als unabhängigen, handlungsrelevanten kardiovaskulären Risikomarker bestätigte – selbst bei Patienten mit normalem LDL-Cholesterinspiegel.
JUPITER within-trial dose-response analysis: participants who achieved hs-CRP below 1 mg/L on rosuvastatin saw a 79% reduction in cardiovascular events — substantially more than those who achieved LDL-C reduction alone, firmly establishing <1 mg/L as the longevity-optimized target.
Meta-Analyse von randomisierten kontrollierten Studien zur mediterranen Ernährung: Die mediterrane Ernährung senkte den hs-CRP-Wert um durchschnittlich 0,98 mg/l; eine ballaststoffreiche Ernährung senkte den hs-CRP-Wert um 28 % – was in seiner Wirksamkeit mit einer Behandlung mit 20 mg Lovastatin pro Tag vergleichbar ist.
Daten zu Hundertjährigen (PMC 2025): Bei Hundertjährigen sind die CRP-Werte im Plasma deutlich niedriger (0,9 ± 0,4 mg/l) als bei Senioren mittleren Alters (2,8 ± 1,6 mg/l), wobei diese Unterschiede auch nach Berücksichtigung von Begleiterkrankungen bestehen bleiben.
Quellen:
Ridker PM et al. Rosuvastatin zur Vorbeugung vaskulärer Ereignisse bei Männern und Frauen mit erhöhtem C-reaktivem Protein (JUPITER). N Engl J Med. 2008;359(21):2195–207.
Ridker PM, Danielson E, Fonseca FA et al. Senkung des C-reaktiven Proteins und des LDL-Cholesterins sowie der Rate kardiovaskulärer Ereignisse nach Beginn der Behandlung mit Rosuvastatin: eine prospektive Studie der JUPITER-Studie. The Lancet. 2009;373(9670):1175-1182. doi:10.1016/S0140-6736(09)60447-5
Ridker PM et al. Entzündungshemmende Therapie mit Canakinumab bei atherosklerotischen Erkrankungen (CANTOS). N Engl J Med. 2017;377(12):1119–31.
Ridker PM et al. C-reaktive Proteinwerte und Behandlungsergebnisse nach einer Statintherapie. N Engl J Med. 2005;352(1):20–8.
Keshani M, Rafiee S, Heidari H, Rouhani MH, Sharma M, Bagherniya M. Die mediterrane Ernährung senkt Entzündungen bei Erwachsenen: Eine systematische Übersicht und Metaanalyse randomisierter kontrollierter Studien. Nutr Rev. Online veröffentlicht am 10. November 2025:nuaf213. doi:10.1093/nutrit/nuaf213
Adibi S. Ein konzeptioneller Rahmen für digitale Gesundheit zur Optimierung der Lebenserwartung: Ein entzündungsorientierter Ansatz, der Mikrobiom- und Lebensstildaten integriert – Eine Übersicht und ein Plattformvorschlag. Nutrients. 2026;18(2):231.

Prospektive Daten bringen Homocysteinwerte über 9–10 µmol/L durchweg mit der Mortalität aufgrund von Herz-Kreislauf-Erkrankungen und neurodegenerativen Erkrankungen in Verbindung. Die Evidenzlage für Homocystein ist jedoch komplexer als bei anderen Biomarkern in diesem Artikel.
Nygård et al. (NEJM, 1997): Bei Patienten mit angiographisch bestätigter koronarer Herzkrankheit waren Homocysteinspiegel von 9,0–14,9 µmol/L bereits mit einer Mortalitätsrate von 3,3 verbunden, verglichen mit Werten unter 9 µmol/L – bei Werten ≥ 20 µmol/L stieg dieser Wert auf 9,9.
PMC-Metaanalyse von 12 prospektiven Studien (n = 23.623): Beim Vergleich der höchsten mit den niedrigsten Homocystein-Kategorien stieg die CHD-Sterblichkeit um 66 %, die kardiovaskuläre Sterblichkeit um 68 %, und jeder Anstieg um 5 µmol/L war mit einem Anstieg der CHD-Sterblichkeit um 52 % verbunden.
Wichtiger Vorbehalt bei RCTs: Wegweisende Studien – HOPE-2 (2006), NORVIT (2006) und VITATOPS (2010) – senkten den Homocysteinspiegel im Plasma durch eine B-Vitamin-Supplementierung zwar erfolgreich, konnten jedoch harte kardiovaskuläre Endpunkte wie Herzinfarkt, Schlaganfall oder die Gesamtmortalität größtenteils nicht reduzieren. Eine nachfolgende Metaanalyse von 19 RCTs (n=47.921) ergab, dass eine B-Vitamin-Supplementierung das Schlaganfallrisiko signifikant senkte, nicht jedoch das Risiko für Herz-Kreislauf-Erkrankungen, Herzinfarkt, koronare Herzkrankheit oder die Gesamtmortalität. Dies stellt den Wert von Homocystein als Risikobiomarker nicht in Frage, mahnt jedoch zur Vorsicht bei der Annahme, dass eine pharmakologische Normalisierung allein die Ergebnisse verbessert.
Quellen:
Nygård O. et al. Plasmahomocysteinspiegel und Mortalität bei Patienten mit koronarer Herzkrankheit. N Engl J Med. 1997;337(4):230–6.
Lonn E. et al. Homocystein-senkende Therapie und Behandlungsergebnisse bei Hochrisikopatienten (HOPE-2). N Engl J Med. 2006;354(15):1567–77.
Clarke R. et al. Auswirkungen einer Senkung des Homocysteinspiegels durch B-Vitamine auf Herz-Kreislauf-Erkrankungen, Krebs und ursachenspezifische Mortalität: Metaanalyse von 8 randomisierten Studien. Arch Intern Med. 2010;170(18):1622–31.
Homocysteine Studies Collaboration. Homocystein und das Risiko für ischämische Herzerkrankungen und Schlaganfall: eine Metaanalyse. JAMA. 2002;288(16):2015-2022. doi:10.1001/jama.288.16.2015
Peng H et al. Erhöhte Homocysteinspiegel und das Risiko für kardiovaskuläre Mortalität sowie Gesamtmortalität: eine Metaanalyse prospektiver Studien. J Zhejiang Univ Sci B. 2015;16(1):78-86.

IL-6 ist das am besten untersuchte proinflammatorische Zytokin im Zusammenhang mit biologischem Altern („Inflammaging“). Die üblichen Referenzwerte in Laboruntersuchungen basieren auf Bevölkerungsdaten und spiegeln nicht die Werte wider, die mit optimaler Lebenserwartung verbunden sind.
Centenarian cohort data (PMC 2025): centenarians demonstrate significantly reduced plasma IL-6 (1.4 ± 0.6 pg/mL) compared to average-aging elderly individuals (3.2 ± 1.8 pg/mL, p<0.001). These differences persist after controlling for comorbidities, suggesting low inflammatory status is a characteristic feature of exceptional longevity.
Tylutka et al., Frontiers in Immunology (2024, PRISMA meta-analysis): the overall IL-6 concentration was significantly higher in patients with age-related diseases compared to controls (SMD 0.16, p<0.001). IL-6 demonstrated diagnostic utility as an independent predictor of age-related morbidity and mortality in elderly adults.
Mendelsche Randomisierung (npj Genomic Medicine, 2019): Der IL-6-Signalweg zeigte kausale inverse Zusammenhänge mit Vorhofflimmern, Schlaganfall, koronarer Herzkrankheit und abdominalem Aortenaneurysma – und stand in einem positiven Zusammenhang mit dem Alter der Eltern zum Zeitpunkt ihres Todes (Indikator für Langlebigkeit).
Quellenangaben:
Tylutka A. et al. IL-6-, TNF- und IL-1β-Spiegel und altersbedingte Erkrankungen: eine systematische Übersicht und Metaanalyse. Front Immunol. 2024;15:1330386.
Zusammenarbeit (Daten von Hundertjährigen). Ein konzeptioneller digitaler Gesundheitsrahmen zur Optimierung der Lebenserwartung. PMC 2025.
Georgakis MK et al. IL-6-Signalwege bei Herz-Kreislauf-Erkrankungen, immunologischen Störungen und Langlebigkeit. npj Genomic Medicine. 2019.
Adibi S. Ein konzeptioneller Rahmen für digitale Gesundheit zur Optimierung der Lebenserwartung: Ein entzündungsorientierter Ansatz, der Mikrobiom- und Lebensstildaten integriert – Eine Übersicht und ein Plattformvorschlag. Nutrients. 2026;18(2):231.

IGF-1 ist komplexer als die meisten Biomarker – ein höherer Wert ist keineswegs besser. Der Zusammenhang mit der Lebenserwartung verläuft U-förmig: Sowohl sehr niedrige als auch sehr hohe Werte bergen ein erhöhtes Risiko, während der mittlere Bereich mit der niedrigsten Sterblichkeitsrate verbunden ist.
Longo et al., Aging Cell (2022) – Metaanalyse von 19 prospektiven Kohortenstudien (n = 30.876): Die Dosis-Wirkungs-Analyse ergab einen U-förmigen Zusammenhang zwischen IGF-1 und der HR für die Gesamtmortalität. Der Bereich von 120–160 ng/ml war mit der niedrigsten Mortalität verbunden. Beim Vergleich von niedrigen mit mittleren IGF-1-Werten zeigte sich eine signifikant erhöhte Gesamtmortalität (HR = 1,33, 95 % KI: 1,14–1,57); auch bei hohen im Vergleich zu mittleren Werten war die Mortalität erhöht (HR = 1,23, 95 % KI: 1,06–1,44).
EPIC-Heidelberg (Mukama et al., J Clin Endocrinol Metab, 2023, bevölkerungsbasierte prospektive Studie): Ein höherer IGF-1-Spiegel stand in direktem Zusammenhang mit dem Risiko für Brustkrebs (HR 1,25) und Prostatakrebs (HR 1,31). Sowohl bei den niedrigsten als auch bei den höchsten IGF-1-Werten bestand ein erhöhtes Risiko für Todesfälle durch Krebs, Herz-Kreislauf-Erkrankungen und alle Ursachen – was die U-förmige Beziehung in einer großen europäischen Population bestätigt.
Das Fazit in der Praxis: Strebe einen physiologisch normalen IGF-1-Spiegel an – was in der Regel durch eine ausreichende, aber nicht übermäßige Proteinzufuhr, regelmäßige Bewegung und gesunden Schlaf erreicht wird – und nicht durch eine medikamentöse Optimierung der GH/IGF-1-Achse.
Quellen:
Rahmani J. et al. Zusammenhang zwischen IGF-1-Spiegeln und der Gesamtmortalität: eine Metaanalyse. Aging Cell. 2022;21(2):e13540.
Mukama T. et al. IGF-1 und das Risiko für Morbidität und Mortalität aufgrund von Krebs, Herz-Kreislauf-Erkrankungen und allen Ursachen in der EPIC-Heidelberg-Studie. J Clin Endocrinol Metab. 2023;108(10):e1092–e1105.

Die stichhaltigsten Belege stammen aus einer IPD-Metaanalyse aus dem Jahr 2023, die in „Lancet Diabetes & Endocrinology“ veröffentlicht wurde – einer der größten Studien zur Schilddrüsenfunktion, die je durchgeführt wurden. Diese Studie hatte ausdrücklich zum Ziel, optimale TSH- und FT4-Bereiche auf der Grundlage klinischer Ergebnisse statt statistischer Bevölkerungsperzentile zu definieren.
Xu et al., Lancet Diabetes & Endocrinology (2023), n = 134.346, durchschnittliche Nachbeobachtungszeit 11,5 Jahre: Es wurden nichtlineare Zusammenhänge für TSH festgestellt, wobei das 60. bis 80. Perzentil (Median 1,90–2,90 mIU/L) mit dem geringsten Risiko für Herz-Kreislauf-Erkrankungen und Mortalität verbunden war. FT4 zeigte einen J-förmigen Zusammenhang, wobei das 20.–40. Perzentil (Median 13,5–14,8 pmol/L) das geringste Risiko aufwies. FT4 im 80.–100. Perzentil war im Vergleich zum optimalen Bereich mit einem 1,34-fachen Anstieg der Gesamtmortalität und einem 1,57-fachen Anstieg der kardiovaskulären Mortalität verbunden.
Interpretation: Der für eine optimale Lebenserwartung ideale TSH-Wert liegt weder am unteren Ende (das mit einer subklinischen Schilddrüsenüberfunktion und einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen und Mortalität verbunden ist) noch an der herkömmlichen Obergrenze von 4,0 mIU/L. Im TSH-Bereich von 1,9–2,9 mIU/L – den die meisten Ärzte derzeit als unauffällig normal einstufen würden – ist das Mortalitätsrisiko am niedrigsten. Insbesondere bei älteren Menschen kann ein TSH-Wert im oberen Normbereich eher adaptiv als pathologisch sein.
Quellen:
Xu Y. et al. Die optimalen Normalwerte der Schilddrüsenfunktion, definiert anhand des Risikos für Herz-Kreislauf-Erkrankungen und Mortalität: Systematische Übersicht und Metaanalyse individueller Teilnehmerdaten. Lancet Diabetes Endocrinol. 2023;11(10):743–754. PMID: 37696273.
Razvi S. et al. Die positive Wirkung von L-Thyroxin auf kardiovaskuläre Risikofaktoren, die Endothelfunktion und die Lebensqualität bei subklinischer Hypothyreose. J Clin Endocrinol Metab. 2007;92(5):1715–23.

Standardlabore stufen Testosteronwerte erst ab dem unteren Bevölkerungsgrenzwert als „niedrig“ ein – ein statistischer, nicht aber ein gesundheitsoptimierter Schwellenwert. Die Langlebigkeitsmedizin ist weniger daran interessiert, „niedrige“ Werte zu vermeiden, sondern konzentriert sich vielmehr darauf, Werte aufrechtzuerhalten, die mit Stoffwechselgesundheit, Erhalt der Muskelmasse, Insulinsensitivität und Schutz der kognitiven Funktionen in Verbindung stehen – typischerweise der obere Mittelbereich für das jeweilige Alter.
The Testosterone Trials (TTrials, NEJM 2016): in men 65+ with low testosterone (<275 ng/dL), testosterone treatment improved sexual function, physical function, and quality of life, with additional signals for bone density and anemia. Metabolic benefits were observed at levels in the mid-normal range.
Quellen:
Snyder PJ et al. Auswirkungen einer Testosteronbehandlung bei älteren Männern (TTrials). N Engl J Med. 2016;374(7):611–24.
Araujo AB, Dixon JM, Suarez EA, Murad MH, Guey LT, Wittert GA. Klinischer Überblick: Endogenes Testosteron und Mortalität bei Männern: eine systematische Übersicht und Metaanalyse. J Clin Endocrinol Metab. 2011;96(10):3007-3019. doi:10.1210/jc.2011-1137

Die Schulmedizin greift erst bei einem eGFR-Wert unter 60 ml/min/1,73 m² ein. In der Langlebigkeitsforschung ist man sich bewusst, dass selbst ein subklinischer Rückgang im Bereich von 60 bis 89 das Risiko für Herz-Kreislauf-Erkrankungen und die Gesamtsterblichkeit deutlich erhöht, weshalb ein Wert von >90 eher ein aktives Ziel als ein irrelevanter Richtwert ist.
CKD-Prognose-Konsortium (Lancet, 2010, n => 1,1 Millionen): Es bestand ein kontinuierlicher, unabhängiger und gradierter Zusammenhang sowohl zwischen einem verminderten eGFR-Wert als auch einer erhöhten Albuminurie und der Gesamtmortalität, der kardiovaskulären Mortalität sowie dem Nierenversagen – wobei ein signifikantes erhöhtes Risiko bereits bei einem eGFR-Wert unter 75 ml/min/1,73 m² auftrat, nicht erst ab dem CKD-Schwellenwert von 60.
Quellen:
Matsushita K. et al. Zusammenhang zwischen der geschätzten glomerulären Filtrationsrate und der Albuminurie mit der Gesamtmortalität und der kardiovaskulären Mortalität in Kohorten der Allgemeinbevölkerung: eine gemeinsame Metaanalyse. Lancet. 2010;375(9731):2073–81.

Die Daten aus klinischen Studien zu Vitamin D waren bisher eher gemischt, doch die Belege für den Zielwert von 40–60 ng/ml haben sich durch aktuelle randomisierte kontrollierte Studien deutlich verstärkt.
TARGET-D-RCT (2024): Bei Hochrisikopatienten senkte eine Vitamin-D-Supplementierung, die auf Werte über 40 ng/ml eingestellt wurde, das Risiko für erneute Herzinfarkte signifikant – eine der ersten randomisierten kontrollierten Studien, die einen kardiovaskulären Nutzen nachweisen konnte, der speziell mit dem Erreichen eines Zielwerts von über 40 ng/ml verbunden ist.
VITAL-RCT (NEJM, 2019, n = 25.871): Während die primären Endpunkte nicht signifikant gesenkt wurden, zeigten vorab festgelegte Analysen eine signifikante Senkung der Krebssterblichkeit bei Teilnehmern mit niedrigem BMI – wobei Post-hoc-Analysen durchweg auf einen größeren Nutzen hindeuteten, wenn die 25-OH-D-Spiegel über 40 ng/ml gehalten wurden.
Quellen:
Manson JE et al. Vitamin-D-Präparate und die Prävention von Krebs und Herz-Kreislauf-Erkrankungen (VITAL). N Engl J Med. 2019;380(1):33–44.
Scragg R. et al. Wirkung einer monatlichen hochdosierten Vitamin-D-Supplementierung auf Herz-Kreislauf-Erkrankungen in der ViDA-Studie. JAMA Cardiol. 2017;2(6):608–16.
TARGET-D-Studie. Titrierte Vitamin-D-Supplementierung und kardiovaskuläre Endpunkte. 2024.

Die Anti-Aging-Medizin beobachtet beide Enden des Ferritin-Spektrums. Ein chronisch erhöhter Ferritinspiegel – selbst innerhalb der herkömmlichen „normalen“ Obergrenze – wird mit oxidativem Stress, Eisenüberladung, nichtalkoholischer Fettlebererkrankung und kardiovaskulären Risiken in Verbindung gebracht.
Daten der UK Biobank und prospektiver Kohortenstudien: Ein Serumferritinwert im oberen Normbereich (>200 ng/ml bei Männern) war mit einem erhöhten Risiko für Lebererkrankungen, das metabolische Syndrom, kardiovaskuläre Ereignisse und die Gesamtmortalität verbunden – unabhängig vom CRP –, was darauf hindeutet, dass eher eine echte Eisenüberladung als ein entzündungsbedingter Ferritinanstieg als ursächlicher Faktor eine Rolle spielt.
Quellen:
Ellervik C, Mandrup-Poulsen T, Andersen HU et al. Erhöhte Transferrinsättigung und Diabetesrisiko: Drei bevölkerungsbasierte Studien. Diabetes Care. 2011;34(10):2256-2258. doi:10.2337/dc11-0416
Ellervik C, Marott JL, Tybjærg-Hansen A, Schnohr P, Nordestgaard BG. Gesamtmortalität und ursachenspezifische Mortalität bei mäßig und deutlich erhöhten Ferritin-Konzentrationen: Bevölkerungsstudie und Metaanalyse. Clin Chem. 2014;60(11):1419-1428. doi:10.1373/clinchem.2014.229013
Mainous AG 3. et al. Erhöhte Serumferritinwerte sind mit einem erhöhten Risiko für Typ-2-Diabetes verbunden. J Am Board Fam Med. 2005;18(3):174–81.
Kadoglou NPE, Biddulph JP, Rafnsson SB, Trivella M, Nihoyannopoulos P, Demakakos P. Der Zusammenhang zwischen Ferritin und der kardiovaskulären Mortalität sowie der Gesamtmortalität bei der Allgemeinbevölkerung: Die englische Längsschnittstudie zum Altern. PLOS ONE. 2017;12(6):e0178994. doi:10.1371/journal.pone.0178994
† Die Hinweise aus Beobachtungsstudien zum Homocystein sind stark; die Evidenz aus randomisierten kontrollierten Studien ist schwach. Details findest du in Abschnitt 3.
WICHTIGE KLINISCHE HINWEISE
Einige dieser Marker weisen eine J-förmige oder U-förmige Beziehung zur Sterblichkeit auf (HbA1c, Harnsäure, IGF-1, TSH) – das heißt, sowohl sehr hohe als auch sehr niedrige Werte bergen ein Risiko. Das Ziel ist die physiologische Optimierung, nicht die isolierte Maximierung oder Minimierung eines Wertes.
Im Bereich der Langlebigkeit wird zunehmend unterschieden zwischen dem epidemiologischen Zusammenhang eines Biomarkers mit der Langlebigkeit und dem durch randomisierte kontrollierte Studien belegten Nutzen einer pharmakologischen Beeinflussung dieses Biomarkers. Bei einigen Markern (Homocystein, HbA1c bei etablierten Diabetikern) weichen diese Werte erheblich voneinander ab. Wo immer möglich, sollten optimale Werte eher durch eine Änderung des Lebensstils – Ernährung, Bewegung, Schlaf und Stoffwechselgesundheit – als allein durch eine medikamentöse oder supplementäre Therapie angestrebt werden.
Dieses Dokument spiegelt den aktuellen Wissensstand von 2024–2025 wider. Referenzbereiche und therapeutische Grenzwerte unterliegen einem ständigen Wandel; Ärzte sollten alle hier dargestellten Zielwerte unter Berücksichtigung der individuellen Situation des jeweiligen Patienten anwenden.